Selbstkontrolle durch punktuelle Blutzuckermessungen
Selbstkontrolle mit Blutzuckermessgeräten und Teststreifen
Angesichts der Möglichkeiten, die das kontinuierliche Glukosemonitoring (rtCGM) bietet, erscheint die kapilläre Blutglukosemessung (SMBG) rudimentär, ist sie aber bei Weitem nicht. Schließlich kann nicht jeder Patient ein CGM-Systenm dauerhaft verwenden, insbesondere, wenn keine Insulintherapie durchgeführt wird. Letztendlich steckt dahinter auch ein ökonomischer Aspekt: der Preis für Blutglukoseteststreifen liegt bei ca. 30 – 50 Cent pro Messung, bei 5 Messungen am Tag also zwischen 1,50 bis 2,50 Euro/Tag, für rtCGM dagegen je nach CGM-System zwischen 5 – 10 Euro/Tag. Auch wenn die Nutzung von rtCGM ständig zunimmt (weltweit aktuell über 10 Millionen Nutzer [1]), ein großer Teil der Diabetespatienten misst nach wie die Blutglukose auf die klassische Weise: mit Blutzuckermessgeräten und TeststreifenVerfahren zur Bestimmung der Glukose im kapillären Blut
Als invasive Methode ist SMBG auf die Entnahme von kleinen Blutproben angewiesen. Die darin enthaltene Glukose wird mit Hilfe von Biokatalysatoren, also speziellen Enzymen chemisch umgewandelt [2,3]. Die gängigen und auch in der Vergangenheit angewendeten Verfahren der enzymatischen Glukosebestimmung sind zu unterscheiden:- nach dem verwendeten Enzym und der darauffolgenden chemischen Reaktion:
– Glukosedehydrogenase (GDH)
– Hexokinase (HK)
- nach der sich aus der Reaktion ergebenden Messgröße:
– Bestimmung der bei der Reaktion umgesetzten Elektronen (amperometrische Messung)
Blutglukosemessung mit Glukoseoxidase (GOD)
Hexokinase (HX) ist dabei eher der Laborchemie vorbehalten. Von der nachgeschalteten Reaktion hat sich besonders die amperometrische Methode erhalten, u.a. auch, weil sie wartungsarm ist. Im einfachsten Fall bei Verwendung des Enzyms Glukoseoxidase (GOD) sorgt dieses in einer ersten Reaktion für eine beschleunigte Oxidation von Glukose. Als Reaktionsprodukte entstehen die Stoffe Glukonolacton und Wasserstoffperoxid H2O2:
Bei Anwendung der elektrochemischen Methode erfolgt in einer zweiten Reaktion im einfachsten Fall die Zersetzung des Wasserstoffperoxids an einer Elektrode, an welche eine elektrische Spannung im Millivoltbereich angelegt ist. Dadurch kommt es zum Übergang von Elektronen vom Wasserstoffperoxid (H2O2) an diese Elektrode:
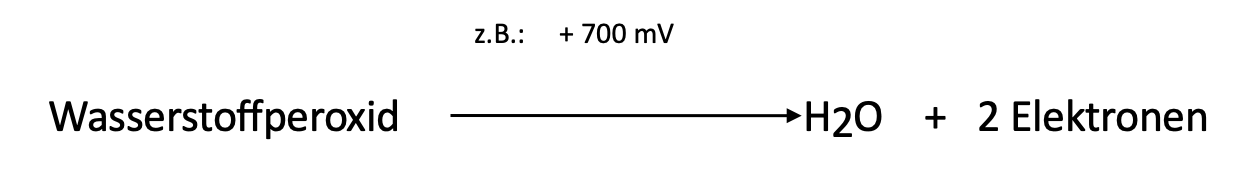
Die freigesetzten Elektronen sorgen für einen kleinen Strom. Dessen Stärke ist umso größer, je mehr Elektronen vorhanden sind. Da die entstandenen Elektronen von der Menge der bei der chemischen Reaktion umgewandelten Glukose abhängig sind, ergibt sich aus der Messung des Stromflusses der Wert für die Blutglukose.
Blutglukosemessung mit Glukosedehydrogenase (GDH)
Die enzymatische Messmethode hat sich in den letzten Jahrzehnten deutlich weiterentwickelt. Der Grund bestand in den sich für die Selbstmessung unter Alltagsbedingungen ergebenden Forderungen. Unter anderem werden überwiegend Teststreifen mit Glukosedehydrogenase (GDH) genutzt. Im Vergleich dazu kann es bei der Messung mit Glukoseoxidase (GOD) zu Interferenzen gegenüber reduzierenden Substanzen und Medikamenten (z. B. Ascorbinsäure, Paracetamol, Blutsauerstoffgehalt) kommen.Bei modernen Systemen zur kapillären Blutzuckermessung (SMBG) verringerten sich die zur Messung notwendigen Blutmengen auf ≤ 0,5 µl, die Messzeiten verkürzten sich auf wenige Sekunden (≤ 5s), äußere Einflüsse wurden kompensiert (Hämatokritabweichungen, Umgebungstemperatur, Sauerstoffpartialdruck usw.) [4-7] und generell hat sich die Handhabung stetig vereinfacht. Allerdings ist die Reaktionschemie mit Glukosedehydrogenase (GDH) komplizierter, weil meist zusätzlich noch ein weiteres Enzym (ein sogenanntes Koenzym) und oft auch ein Mediator eingesetzt werden muss [7]. Als Beispiel sei die Verwendung des Koenzyms Nicotinamidadenindinukleotid (NAD) angeführt, mit folgenden Reaktionen:

Bei der an zweiter Stelle aufgeführten Reaktion des reduzierten Koenzyms mit einem Mediator werden Elektronen frei, die an die Elektrode des Teststreifens fließen. Der entstehende Stromfluss ist wiederum abhängig von der Menge der bei der Reaktion umgewandelten Glukose und gibt Auskunft über die Höhe der Blutglukose.
Ein wichtiger Vorteil ist, dass an die Elektrode nur eine sehr kleine Spannung angelegt werden muss, wodurch Nebenreaktionen mit anderen Substanzen des Körpers vermieden werden. Die Spezifik für den Nachweis von Glukose ist folglich besser, womit die erwünschten Verbesserungen zum Tragen kommen (geringe Blutmengen, Unabhängigkeit vom Sauerstoff usw.).
Bluzuckermessgeräte unterscheiden sich kaum
Die Testverfahren der verschiedenen Anbieter von Blutglukosemessgeräten unterscheiden sich vor allem bezüglich der chemischen Bestimmung und damit der Teststreifen. Natürlich unterscheiden sich auch die Blutglukosemessgeräte. Das Design spielt dabei ebenso eine Rolle wie das Gefühl beim Handling. Von diesbezüglichen Details (Größe der Bedienungsfelder, Größe des Displays, usw.) abgesehen, ist die grundsätzliche Handhabung bei den verschiedenen Blutglukosemessgeräte vergleichbar: der Teststreifen wird in das Gerät eingeführt, dabei schaltet sich das Gerät ein, das aufgetragene Blut wird aufgesaugt, eine Nachdosierung ist möglich, nach kurzer Zeit wird der Glukosewert angezeigt.Kalibierung von Blutzuckermessgeräten nicht mehr notwendig
Die Fragen z.B. nach der Genauigkeit der Messung, der Messdauer und der Blutmenge wird auf dem Teststreifen entschieden. Nach der enzymchemischen Reaktion entsteht ein Stromfluss, der mit dem integrierten Ampermeter gemessen und in einen Glukosewert umgerechnet wird. Weiterhin werden die gängigsten Blutglukosemessgeräte seitens der Hersteller kalibriert. Dass mit einem Testchip o.ä. kalibriert wird ist äußerst selten. Es ist aber möglich die Messgenauigkeit der Geräte zu überprüfen, indem eine für das jeweilige Gerät spezifische Kontrolllösung auf den Teststreifen aufgetragen wird.Zu den Innovationen bei der Blutglukosemessung zählen auch die Hilfsmittel zur Blutentnahme. Diese wurden häufig verbessert: Lanzetten mit Facettenanschliff, welche das Gewebe exakt schneiden und longitudinal geführte Stechhilfen, welche beim schnellen und kurzen Einschlag in das Gewebe keine laterale Abweichung aufweisen. All das führt zu einer schmerzarmen Blutentnahme. Zusammen genommen verringerten alle Verbesserungen deutlich Fehlmessungen.
Apps und Software für das Diabetesmanagement
Grundsätzlich kann die Entwicklung von SMBG als weitgehend abgeschlossen betrachtet werden. Die Methode entspricht technisch dem aktuell denkbaren möglichen Standard.Es gibt aber auch außerhalb der eigentlichen Messmethode Innovationen, welche die Messgeräte betreffen. Sie profitieren wie viele andere Systeme von der allgemeinen Entwicklung der Digitalisierung. Im Fall der Blutglukosemessung geht es dabei vor allem um die Auswertung und Beurteilung der Daten. Zu den Messsystemen gehören Softwarelösungen, insbesondere solche, die über Smartphone-Apps laufen und so eine für die therapeutische Beurteilung und Therapiesteuerung unmittelbare und einfache Anwendung bieten. Aktuelle Beispiele sind die Verbindung von SmartPens mit Apps, wie zum Beispiel NovoPen6 und NovoPen Echo (beide Novo Nordisk) oder InPen (Medtronic) [8,9].Messgenauigkeit von Blutglukosemesssystemen für die punktuelle Blutglukosemessung
Die Genauigkeit von Blutglukosemesssystemen ist wichtig, damit Therapieentscheidungen getroffen werden können und eine sichere Verlaufskontrolle ermöglicht wird. Für die Hersteller und Inverkehrbringer solcher Systeme bedeutet dies, dass sie die Norm zur Systemgenauigkeit, die ISO 15197:2015 einhalten müssen [10]. Das bedeutet, dass bei einem Blutglukosewert unter 100 mg/dl (5,5 mmol/l) 95 % der gemessenen Werte innerhalb eines Schwankungsbereichs von +/- 15 mg/dl (0,83 mmol/l) liegen müssen. Oberhalb dieses Bereiches von 100 mg/dl (5,5 mmol/l) dürfen sie nur eine Toleranz von +/- 15 % aufweisen [10]. Abb. SK 2 zeigt dafür ein Beispiel [11]. Zusätzlich sind gewisse Anforderungen zur erfüllen, so z.B. die sichere Handhabung betreffend oder die Minimierung von äußeren Einflussfaktoren.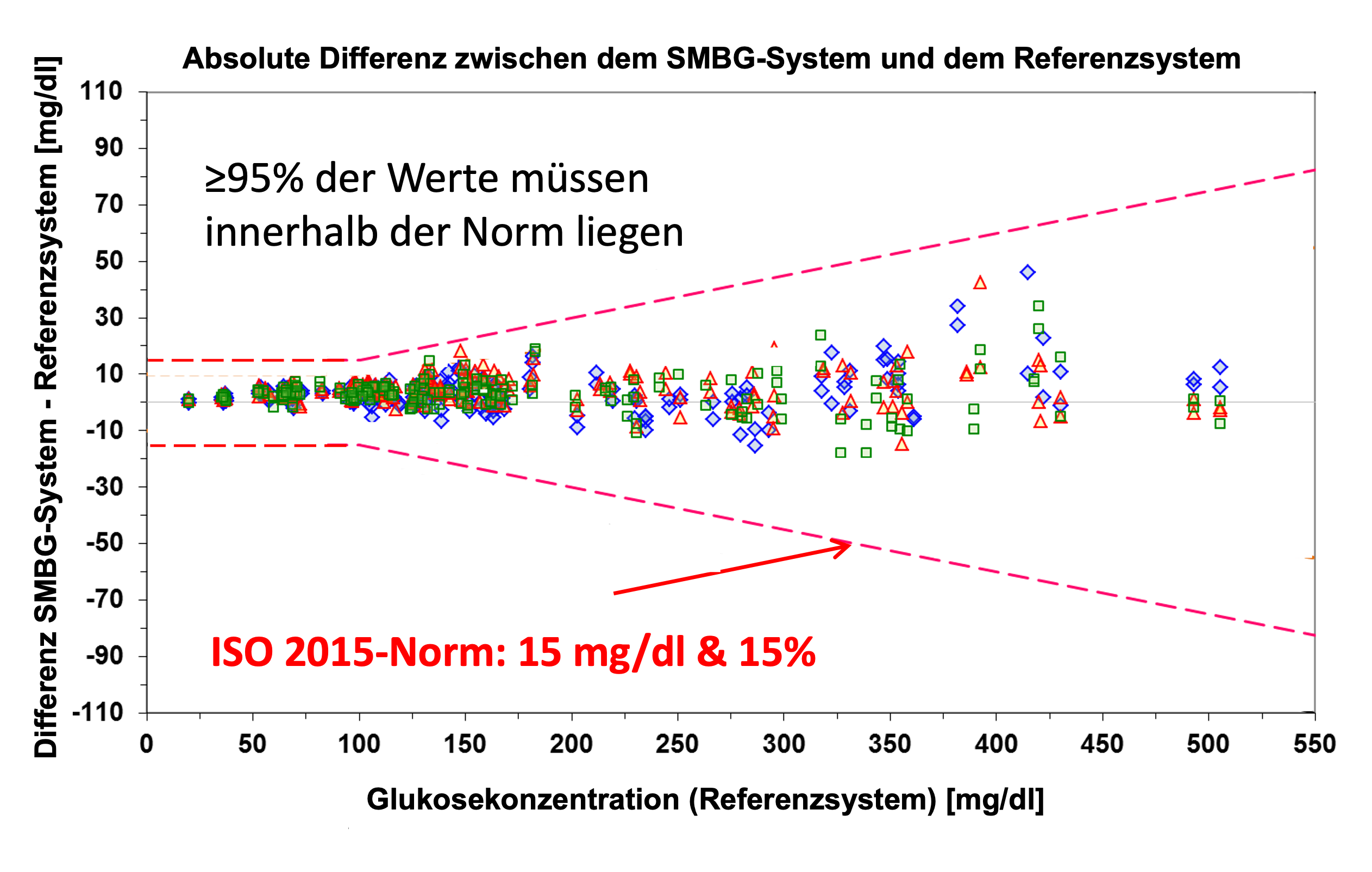
Abb. SK 2: Beispiel für die Genauigkeitsbestimmung von mehreren Blutglukosemessgeräten nach den Systemgenauigkeitsnorm ISO 15197:2015 [modifiziert nach [11]).
Beurteilung nach der Error-Grid-Analyse
Zur Beurteilung der Genauigkeit von Glukosemessgeräten in Bezug auf eine Referenzglukosemessung dient auch die Error-Grid-Analyse. Dabei handelt es sich um eine Fehlerrasteranalyse, die für Glukosedaten modifiziert wurde. Sie beantwortet die Frage nach der klinischen Relevanz von abweichenden Glukosedaten im Rahmen der Diabetestherapie (klinische Genauigkeit). Das heißt die Abweichung eines Messwertes zum Referenzmesswert wird anhand der sich für die Diabetesbehandlung ergebenden Folgen betrachtet. Diese Spezifizierung wurde zuerst von W. Clarke in den 1980er Jahren entwickelt, weshalb die grafische Darstellung als Clark-Error-Grid-Plot (EGP) bezeichnet wird [12] (Abb. SK 3, links).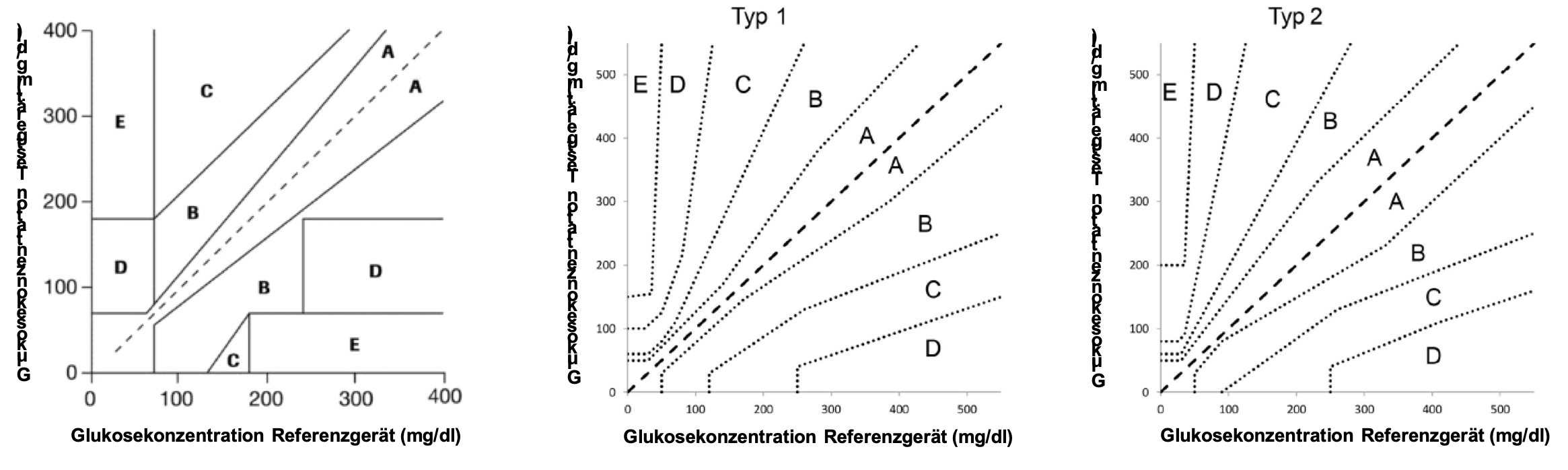 Abb. SK 3: Error-Grid-Plots nach Clarke [12] (links) und nach Parkes [13] (Mitte für Typ-1-Diabetes, rechts für Typ-2-Diabetes).
Abb. SK 3: Error-Grid-Plots nach Clarke [12] (links) und nach Parkes [13] (Mitte für Typ-1-Diabetes, rechts für Typ-2-Diabetes).In das Raster (Abb. SK 3) werden die paarweise gemessenen Werte von einer Probe (Glukosekonzentration von Testgerät und Referenzgerät) eingetragen. Bei 100%iger Übereinstimmung liegt diese Werte genau auf der Winkelhalbierenden der Darstellung. Eine Vielzahl von Glukosewertepaaren ergibt dann in der Grafik eine gewisse Verteilung. In der Grafik sind fünf verschiedene Zonen festgelegt, entsprechend ihrer klinischen Relevanz unterschieden:
- Zone A: alle Werte, die eine maximale Abweichung von 20% vom Referenzwert aufweisen (klinisch akkurat).
- Zone B: Werte mit einer Abweichung > 20% vom Referenzwert, die aber keine fehlerhafte Auswirkung auf die Therapie des Patienten haben (klinisch günstig).
- Zone C: abweichende Werte, die ungünstige aber noch keine gefahrbringenden therapeutische Entscheidungen zur Folge haben (klinisch noch ausreichend).
- Zone D: Werte, deren Abweichung gefährliche Fehlerentscheidungen, speziell bei der Erkennung einer Hypo- oder Hyperglykämie hervorrufen können (klinisch fehlerhaft).
- Zone E: Werte, die derart voneinander abweichen, dass eine Hypoglykämie oder Hyperglykämie nicht mehr zu unterscheiden und folglich zu einer grob falschen Behandlung führen würde (klinisch falsch). Im günstigsten Fall liegt der Großteil der Werte in der Zone A, also auf beiden Seiten der Mittelhalbierenden des EGP. Das trifft auf die meisten Blutglukosemessgeräte zu. Gegeben falls liegt ein geringer Anteil in Zone B.
Charakteristik der Blutprobe bei der Blutglukose-Selbstmessung (SMBG)
Blut setzt sich aus Blutzellen, also Erythrozyten, Leukozyten, Thrombozyten (Blutplättchen) und Plasma zusammen. Das Plasma besteht zu 90% aus Wasser, Proteinen, Salzen und Nährstoffen und enthält auch die Blutglukose. Blut ist das wichtigste Transportmedium des Organismus. Es transportiert Gase (Sauerstoff, Kohlenstoffdioxid, Stickstoff usw.) ebenso wie Nährstoffe (also auch Glukose) und Endprodukte des Zellstoffwechsels. Das Blut stellt den Austausch von Stoffen im Organismus sicher.Da die Blutglukose-Selbstmessung im Kapillarblut (kapillares Vollblut) durchgeführt wird, wird das Blut „verdünnt“, d.h. der Blutglukosewert ist niedriger, als er bei einer Messung aus dem Plasma, zum Beispiel im Labor wäre. Dieser Effekt beträgt ca. 11%. Alle modernen Messgeräte weisen aber die Ergebnisse plasmakalibriert aus, d.h. sie geben die aktuelle Glukosekonzentration im Blutplasma wieder.
Literatur:
[1] Kelly Close Report 21.01.2025
[2] Hönes J, Müller P, Surridge N. The Technology Behind Glucose Meters: Test Strips. Diabetes Technology & Therapeutics 2008; 10(Suppl.1): S10-S26.
[3] Heinemann L. Measuring glucose concentrations: daily practice, current and future developments. J Diabetes Sci Technol. 2008 Jul;2(4):710-717.
[4] Baumstark A, Liebing C, Jendrike N, Pleus S, Haug C, Freckmann G. Evaluation of Hematocrit Influence on Measurements With a Novel Self-Monitoring of Blood Glucose System Based on ISO 15197:2013. J Diabetes Sci Technol. 2018 Sep;12(5):1078-1079.
[5] Hattemer A, Wardat S. Evaluation of Hematocrit Influence on Self-Monitoring of Blood Glucose Based on ISO 15197:2013: Comparison of a Novel System With Five Systems With Different Hematocrit Ranges. J Diabetes Sci Technol. 2018 Mar;12(2):333-340.
[6] Nerhus K, Rustad P, Sandberg S. Effect of ambient temperature on analytical performance of self-monitoring blood glucose systems. Diabetes Technol Ther. 2011 Sep;13(9):883-892.
[7] Baumstark A, Schmid C, Pleus S, Haug C, Freckmann G. Influence of partial pressure of oxygen in blood samples on measurement performance in glucose-oxidase-based systems for self-monitoring of blood glucose. J Diabetes Sci Technol. 2013 Nov 1;7(6):1513-1521.
[8] Heinemann L, Schnell O, Gehr B, Schloot NC, Görgens SW, Görgen C. Digital Diabetes Management: A Literature Review of Smart Insulin Pens. J Diabetes Sci Technol. 2022 May;16(3):587-595.
[9] MacLeod J, Vigersky RA. A Review of Precision Insulin Management With Smart Insulin Pens: Opening Up the Digital Door to People on Insulin Injection Therapy. J Diabetes Sci Technol. 2023 Mar;17(2):283-289.
[10] DIN EN ISO 15197:2015 DE – Testsysteme für die In-vitro-Diagnostik – Anforderungen an Blutglukosemesssysteme zur Eigenanwendung bei Diabetes mellitus (ISO 15197:2013); Deutsche Fassung EN ISO 15197:2015 (Foreign Standard). Letzter Aufruf: 12.03.2025
[11] Freckmann G, Link M, Schmid C, Pleus S, Baumstark A, Haug C. System Accuracy Evaluation of Different Blood Glucose Monitoring Systems Following ISO 15197:2013 by Using Two Different Comparison Methods. Diabetes Technol Ther. 2015 Sep;17(9):635-48. doi: 10.1089/dia.2015.0085.
[12] Clarke WL, Cox D, Gonder-Frederick LA et.al. Evaluating clinical accuracy of systems for self-monitoring of blood glucose. Diabetes Care. 1987; 10(5):622-628.
[13] Parkes JL, Slatin SL, Pardo S, et.al. A new consensus error grid to evaluate the clinical significance of inaccuracies in the measurement of blood glucose. Diabetes Care. 2000; 23(8):1143-1148.
Kategorisiert in: Selbstkontrolle
Dieser Artikel wurde verfasst von admin










